Grupos de la tabla periódica
(4,5,6 y 7)
Introducción:
La tabla periódica es un instrumento muy importante y familiar para nuestras vidas que forma parte del material didáctico para cualquier estudiante y estudiante de la química, medicina e ingeniería. En la tabla periódica se obtienen datos necesarios de algún elemento determinado, conoceremos la división de la tabla periódica en sus diferentes grupos, específicamente los 4, 5, 6 y 7.
Objetivos:
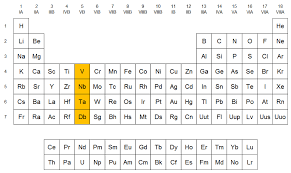
- Conocer la división de la tabla periódica
- Según su división en grupos, conocer específicamente los grupos 4, 5, 6 y 7; teniendo en cuenta sus características y lo elementos que lo componen.
- Tener presente en qué lugar se ubica cada uno de dichos grupos.
La familia o grupo IVA son los carbonoideos, no metales. A medida que se desciende en el grupo, aumenta el carácter metálico de sus componentes. el C y el Si son no metales, el germanio es un semimetal y el Sn junto con el Pb son netamente metálicos. El C y el Si tienden a formar uniones covalentes para completar su octeto electrónico, mientras que el Sn y el Pb tienden a ceder, por su carácter metálico.
Características:
La familia o grupo VA son los no metales nitrogenoideos. El N y el P son no metálicos, el arsénico y el antimonio son semimetales, a veces se comportan como metales y otras como no metales (esto es carácter anfótero). El Bi es un metal. esta variación de no metálico a metálico, a medida que se avanza en el grupo, se debe al aumento del tamaño de los átomos. resulta más difícil separar un electrón del átomo de N que hacerlo con el de Bi, porque en el primero la atracción nuclear es más intensa. Las moléculas de N son biatómicas, el P, As, Sb presentan moléculas tetratómicas en algunos de sus estados alotrópicos. el Bi es biatómico. todos estos elementos forman enlaces covalentes.
Características:
La familia o grupo VIA son los no metales calcógenos. Sus puntos de fusión, densidad y ebullición aumentan a medida que se desciende en el grupo, es decir a medida que aumenta el tamaño de los átomos. Se combinan con el H para formar hidruros no metálicos. De acuerdo a la electronegatividad, la afinidad química con el H decrece del O al Te. Cuando se combinan con el H, su número de oxidación de -2, pero cuando lo hacen con elementos más electronegativos presentan numero de oxidación positivo (4 , 6)
Características:
Características:
ANEXOS:
- Video en youtube: https://www.youtube.com/watch?v=JJJBqiZy-Hs
Webgrafía:
- https://www.areaciencias.com/quimica/familias-de-la-tabla-periodica.html
- https://prezi.com/y_hyqcvfm_5n/caracteristicas-de-los-grupos-de-la-tabla-periodica/










No hay comentarios:
Publicar un comentario